香港科技大学深圳研究院生物材料转化实验室
【研发团队】
团队带头人:

周迎教授,香港科技大学化学生物工程系副教授,生物工程研究生课程副主任,香港科技大学深圳研究院副教授;分别担任香港生物科技协会的副主席及理事会成员,美国眼科与视觉研究协会(ARVO)会员,美国药物缓释协会(CRS)会员及美国化学工程院会员。
周迎教授毕业于麻省理工大学,师从生物材料的鼻祖Robert Langer教授,其有关癌症靶向治疗的博士论文获得安进公司(Amgen Inc.)的资助。周教授有14年生物材料及药物递送系统的研究经验,其研究团队已发表超过35篇论文,引用次数超过550次。
周教授曾经在美国默克公司工作四年,在生物制药,技术转移,GMP生产等方面有一手经验。周教授于2006年加入香港科技大学后,成功领导了多个生物材料或药物递送系统相关的研究,获得超过一千万港币的科研经费资助。周教授实验组关于可注射长效缓释凝胶的研究在生物材料界以及临床眼科界都受到广泛关注,曾多次应邀在学术会议或眼科医院进行学术报告,包括第七届国际材料及先进技术大会(the 7th International Conference on Materials for Advanced Technologies),香港国际生物材料大会(Biomedical Engineering International Conference (Hong Kong)),国际青年先进材料研究人员大会(The International Conference of Young Researchers on Advanced Materials),第27界亚太眼科大会(APAO)等。
实验室团队:
周迎教授课题组从2006年起开始对眼部药物递送系统进行研究。课题组是世界上最先对眼部用超声波进行非介入性蛋白质药物递送系统的研究(Investigative Ophthalmology and Visual Science, 2013)。在纳米科技方面,周教授课题组曾以叶酸修饰纳米颗粒制成色素细胞靶向性抗新生血管药物的缓释剂型(Journal of Controlled Release, 2013)。在眼部药物缓释方面,周教授课题组最先发表了一种高度可控的羟基高分子进行乙烯砜基活化的方法(Biomacromolecules, 2012)。此文章在Biomacromolecules杂志发表后,成为当年最多下载的论文之一。此方法的建立,使其实验组能探索眼后部药物超长时缓释系统的可注射凝胶剂型研究 ,研究小组成员曾经在包括2014美国眼科与视觉研究协会年会(ARVO Conference 2014),第八届国际眼科论坛(8th International Symposium of Ophthalmology),第九届世界生物材料大会(the 9th World Biomaterials Congress),国际眼科药物及药剂学大会(the International Symposium on Ocular Pharmacology and Therapeutics),及第三十八届缓释协会年会(The 38th Annual Meeting and Exposition of the Controlled Release Society)等学术会议宣讲,并发表在Biomacromolecules以及Translational Visual Science and Technology杂志上。其研究团队成员曾获得多项国际科研大奖,包括国际华人生物材料工程大会青年科研人员大奖(Young Investigator Awards), 香港国际生物工程大会年轻工程师论文大赛一等奖等。
【项目简介】
眼健康是国民健康的重要组成部分,包括盲在内的视觉损伤严重影响民众的身体健康和生活质量,加重家庭和社会负担,威胁社会经济生产活动,是涉及民生的重大公共卫生问题和社会问题。现阶段最严重的致盲性疾病是以黄斑病变和糖尿病视网膜病变为代表的眼后部血管新生疾病。在发达国家和地区,此两种疾病的致盲率占所有失明案例的70%,而在中国,黄斑病变的发病率在五十岁人群中高达10%,糖尿病人中患糖尿病视网膜病变的人数超过35%。也正是因为这两种疾病发病率高、病情凶险、治疗难度大,它们成为《“十三五”全国眼健康规划》的防治重点。
现阶段,在临床上对这两种疾病的治疗需要频繁进行抗血管新生蛋白药物的玻璃体内注射。这种治疗方案会对病人带来很大的不适和负担,故而在实际临床实践中病人的依存性较低。重复主色还会增加眼部感染等严重副作用的发生率。本项目将针对目前治疗方式的不足,开发以水凝胶作为蛋白药物的载体的长效缓释体统,最终目标是将治疗黄斑病变与糖尿病视网膜炎的注射频率从每月一次降到每半年或每年一次,减低患者的痛苦及治疗成本。
选择以水凝胶作为蛋白药物的载体,是因为水凝胶富含水分的微环境不仅可以保持蛋白质药物的活性,还可以通过调节孔径大小改变药物释放率以适用于不同的疾病。在前期研究中,我们已开发了一种能在动物体内停留至少6个月的凝胶系统,并初步在兔眼和猴眼中验证了生物相容性。在本研究中,我们将进一步优化凝胶的缓释及降解特性,并在动物模型中验证凝胶制剂的长期疗效,为进入临床研究做进一步的优化。
【重要科研成果】
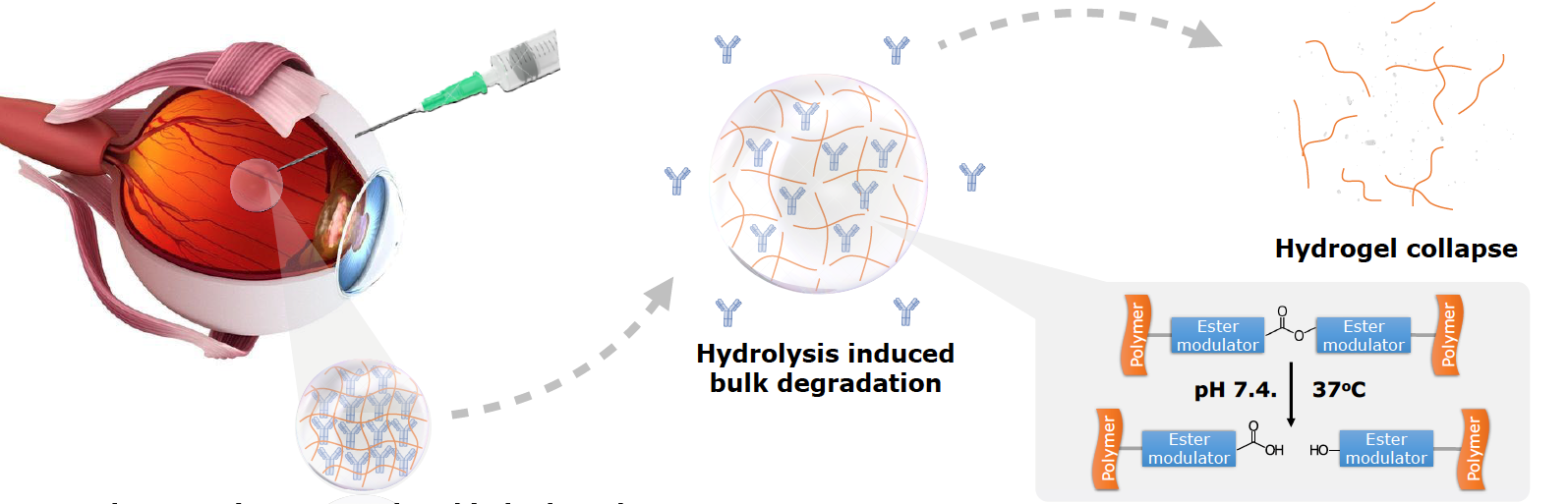
周迎教授团队对可注射凝胶的蛋白质缓释行为进行了长期的理论及实验研究。其创新使用Blob模型对凝胶的网格结构进行模拟及预测,使团队能开发缓释时间超过半年的凝胶。研发团队已经在兔眼及猴眼内验证材料的生物相容性,以及通过与中山眼科中心合作,在全球首次在灵长类动物眼中建成了模拟黄斑病变及糖尿病视网膜病变的继发性脉络膜新生血管模型,并在此模型中验证缓释凝胶的长期疗效。
